��һ�����������Ƕ���壨PROTAC��
PROTAC�ĸ�����������2001����Crews����������ܹ����û�������Ȼ���ڵĵ�������ϵͳ�����͵���ˮƽ�������Ƶ��Ĺ��ܣ��������Ƽ�����Ŀ�ġ�PROTAC��������20��IJ������ƺͷ�չ��ٲȻ��ΪĿǰ��ҩ�з���������ȵļ���֮һ���ܵ�����Ժ����ҩ���Ͷ�ʻ�����������
PROTAC��һ��˫���ܷ��ӣ�һ���ǽ�ϰе��ף�Protein of Interest,POI�������壬��һ���ǽ�Ϸ�������øE3�����壬��������ͨ�����������ӣ�linker��������PROTAC���ӽ���ϸ����һ�˽�ϰе��ף���һ�˽�Ϸ�������øE3���γ�POI-PROTAC-E3��Ԫ���������Ԫ�������ܹ���һ���ٽ����ص��״�E3����ø������ת����Ŀ�군�ı��棬��������ػ����ã�ʹĿ�군���⡣�������С����ҩ����÷�Χ���㡢���Ը��ߡ��ɰ����ɳ�ҩ���е㡣�Ƶ�˼���������������Ͳ���С��������PROTAC���ӵĶ��ƺϳɷ���
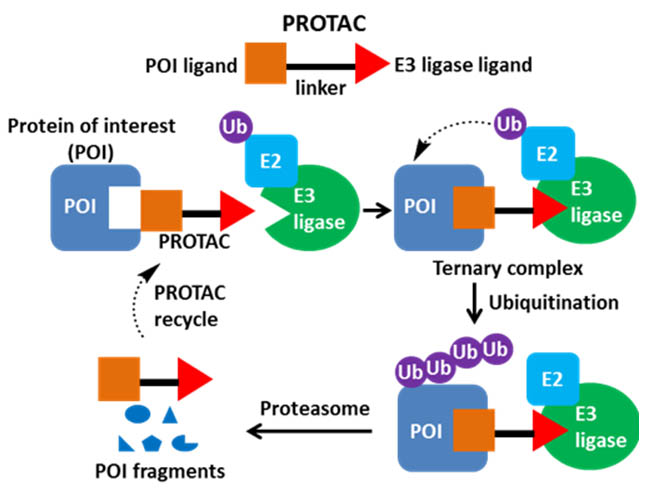
PROTAC��������
�ο����ף�
B��k��s, M., Langley, D. R., & Crews, C. M. (2022). PROTAC targeted protein degraders: the past is prologue. Nature reviews. Drug discovery, 21(3), 181�C200.
https://doi.org/10.1038/s41573-021-00371-6
Zhao, L., Zhao, J., Zhong, K., Tong, A., & Jia, D. (2022). Targeted protein degradation: mechanisms, strategies and application. Signal transduction and targeted therapy, 7(1), 113.
https://doi.org/10.1038/s41392-022-00966-4
��������ø�����Ƕ���壨LYTAC��
LYTAC��һ�����˵�������ø�彵������Ĥ���ļ�������2020����Bertozzi�����״��������Ҳ��һ��˫���ܹ����ͬʱ���ϸ���⵰��ϸ��������ø���������(LTR) �γ���Ԫ��������µ����ʿ���ͨ�����鵼�����������ڻ�������û����������ͨ���������壨EE�����������壨LE�����POI ������ø�彵�⣬�� LTR �����յ�ϸ��Ĥ��ͨ���������壨RE����LYTAC�����ڵ����ӹ���ǰ���併�⣬��˱�����DZ�ڵ���������;���ļ��

Lytac���û����Լ�tri-GalNAc-DBCO����ṹ
LYTAC��һ��˫���ܷ��ӣ�һ���ǽ��POI��С���ӻ��壬��һ���ǽ����ø��������壨LTR�������壬�����������ͨ��linker���ӡ�����Ĥ���γɵ�LTR�CLYTAC�CPOI��Ԫ������ᱻϸ��Ĥ����û�����γ�һ���������ݡ����ݻὫ���������䵽��ø���У��е��ױ����⡣�Ƶ�˼�����ṩ�ʺ϶���ż����ʽ��tri-GalNAc����ϳ��Լ�����LYTAC���ӵĶ��ơ�
�ο����ף�
Ahn, G., Banik, S. M., Miller, C. L., Riley, N. M., Cochran, J. R., & Bertozzi, C. R. (2021). LYTACs that engage the asialoglycoprotein receptor for targeted protein degradation. Nature chemical biology, 17(9), 937�C946. https://doi.org/10.1038/s41589-021-00770-1
Banik, S. M., Pedram, K., Wisnovsky, S., Ahn, G., Riley, N. M., & Bertozzi, C. R. (2020). Lysosome-targeting chimaeras for degradation of extracellular proteins. Nature, 584(7820), 291�C297. https://doi.org/10.1038/s41586-020-2545-9
����������ż��ҩ�PDC��
PDC(Peptide-Drug Conjugate)������ż��ҩ��������ӣ�linker�����鳲�ģ�homing peptide���Լ�����ϸ�����Ե���Ч�غɣ�payload�����ɣ������Ŀ���������������ϸ�����������ĵ�������Ӷ�����ϸ�������յ�����ϸ�������������ĿǰADC ҩ�PDC ҩ����з�����С����������ǿ������ԭ�Ե͡����ù���ϳɷ��ɴ��ģ�ϳɡ������ɱ��ϵ͡���ԽϺõ�ҩ������ѧ���ص㣬��Ϊ��С���Ӱ���ҩ������¡���塢ADC ֮�����һ����������ҩ���Ƶ�˼���ォΪ�ͻ��ṩ�Ӱ�����ĺϳɵ������غ�ż����һվʽPDCҩ��ϳɼ�������
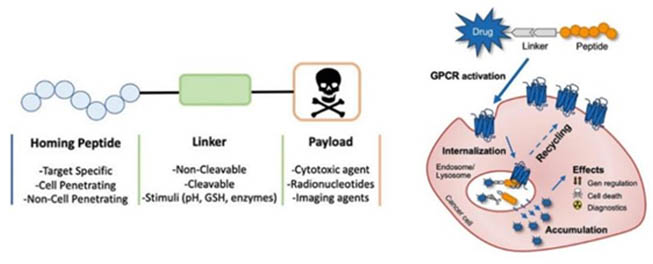
PDC�Ľṹ�����û���
�ο����ף�
Zhu, Y. S., Tang, K., & Lv, J. (2021). Peptide-drug conjugate-based novel molecular drug delivery system in cancer. Trends in pharmacological sciences, 42(10), 857�C869.
https://doi.org/10.1016/j.tips.2021.07.001
Wang, Y., Cheetham, A. G., Angacian, G., Su, H., Xie, L., & Cui, H. (2017). Peptide-drug conjugates as effective prodrug strategies for targeted delivery. Advanced drug delivery reviews, 110-111, 112�C126.
https://doi.org/10.1016/j.addr.2016.06.015
